Sepanta Laser Spadan
شرکت سپنتا لیزر اسپادان سهامی خاصSepanta Laser Spadan
شرکت سپنتا لیزر اسپادان سهامی خاصنظرسنجی
پیوندها
ارتباطات
- تماس با مدیر سایت نظرات و پیشنهادات خود را با مدیر سایت در میان گذارید
دستهها
ابر برجسب
شکوفه ساتری جزوه لیزر جزوه لیزر پزشکی گروه پژوهشی عطفان نژاد و ساتری اپتیک پزشکی جزوه لیزر دندانپزشکی تدریس فیزیک با شکوفه ساتری رشته مهندسی اپتیک و لیزر شرکت سپنتا لیزر اسپادان لیزر توموگرافی انسجام نوری تدریس آناتومی با شکوفه ساتری بیوفوتونیک گروه آموزشی مهندس شکوفه ساتری مهندس شکوفه ساتریبرگهها
جدیدترین یادداشتها
همه- حوزه های تحقیقاتی مهندس ساتری پژوهش حوزه های تحقیقاتی بیومکانیک مهندسی زیست مواد و احیا کننده مهندسی سلول و مولکولی تصویربرداری و بیوفوتونیک تجهیزات...
- اپتیک زیست پزشکی اپتیک زیست پزشکی رشته ای است که اصول اولیه برهمکنش بین نور و بافت های بیولوژیکی، سلول ها و مولکول ها را مطالعه می کند و...
- اپتیک زیست پزشکی فناوری های تصویربرداری نوری زیست پزشکی طراحی و ساخت دستگاه های نوری زیست پزشکی اپتیک بینایی، تصویربرداری و حس کردن چشم...
- بیوفوتونیک با شکوفه ساتری بیوفوتونیک بالینی و ترجمه ای توسعه و کاربرد تکنیک های نوری برای کاربردهای بالینی را پوشش می دهد. میکروسکوپ،...
- راهحلها و نوآوریها را از شرکتهای زیستپزشکی پیشرو در صنعت بیابید بزرگترین نمایشگاه اپتیک و بیوفوتونیک زیست پزشکی جهان است. جدیدترین فناوریها را از شرکتهای برتر ارائهدهنده راهحلهای...
- فناوری جدید هوش مصنوعی ممکن است به کشف عوامل درمانی برای اختلالات عصبی کمک کند یک گروه تحقیقاتی از دانشگاه ناگویا در ژاپن، هوش مصنوعی را برای تجزیه و تحلیل تصاویر سلولی ایجاد کرده است که از یادگیری...
- هدف محققان ایجاد یک الگوریتم هوش مصنوعی برای تشخیص زودهنگام اوتیسم در کودکان است آیا می توان از هوش مصنوعی برای کمک به تشخیص زودهنگام اختلال طیف اوتیسم استفاده کرد؟ این سوالی است که محققان دانشگاه...
- دستگاه جدید حسگر فیبر نوری، نشانگرهای زیستی کلیدی را به دنبال آسیب مغزی تروماتیک نظارت می کند دستگاه جدید حسگر فیبر نوری، نشانگرهای زیستی کلیدی را به دنبال آسیب مغزی تروماتیک نظارت می کند نتایج "امیدبخش"...
- کارآزمایی برتری هوش مصنوعی را در ارزیابی عملکرد قلب نسبت به ارزیابی سونوگرافی نشان می دهد کارآزمایی برتری هوش مصنوعی را در ارزیابی عملکرد قلب نسبت به ارزیابی سونوگرافی نشان می دهد در بیمارانی که تحت ارزیابی...
- هوش مصنوعی در تشخیص عملکرد قلب نسبت به سونوگرافیک ها دقیق تر است هوش مصنوعی در تشخیص عملکرد قلب نسبت به سونوگرافیک ها دقیق تر است در اولین کارآزمایی بالینی تصادفی شده در نوع خود که...
نویسندگان
بایگانی
تقویم
شهریور 1401| ش | ی | د | س | چ | پ | ج |
| 1 | 2 | 3 | 4 | |||
| 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 19 | 20 | 21 | 22 | 23 | 24 | 25 |
| 26 | 27 | 28 | 29 | 30 | 31 |
جستجو
محرک های اپتوژنتیک
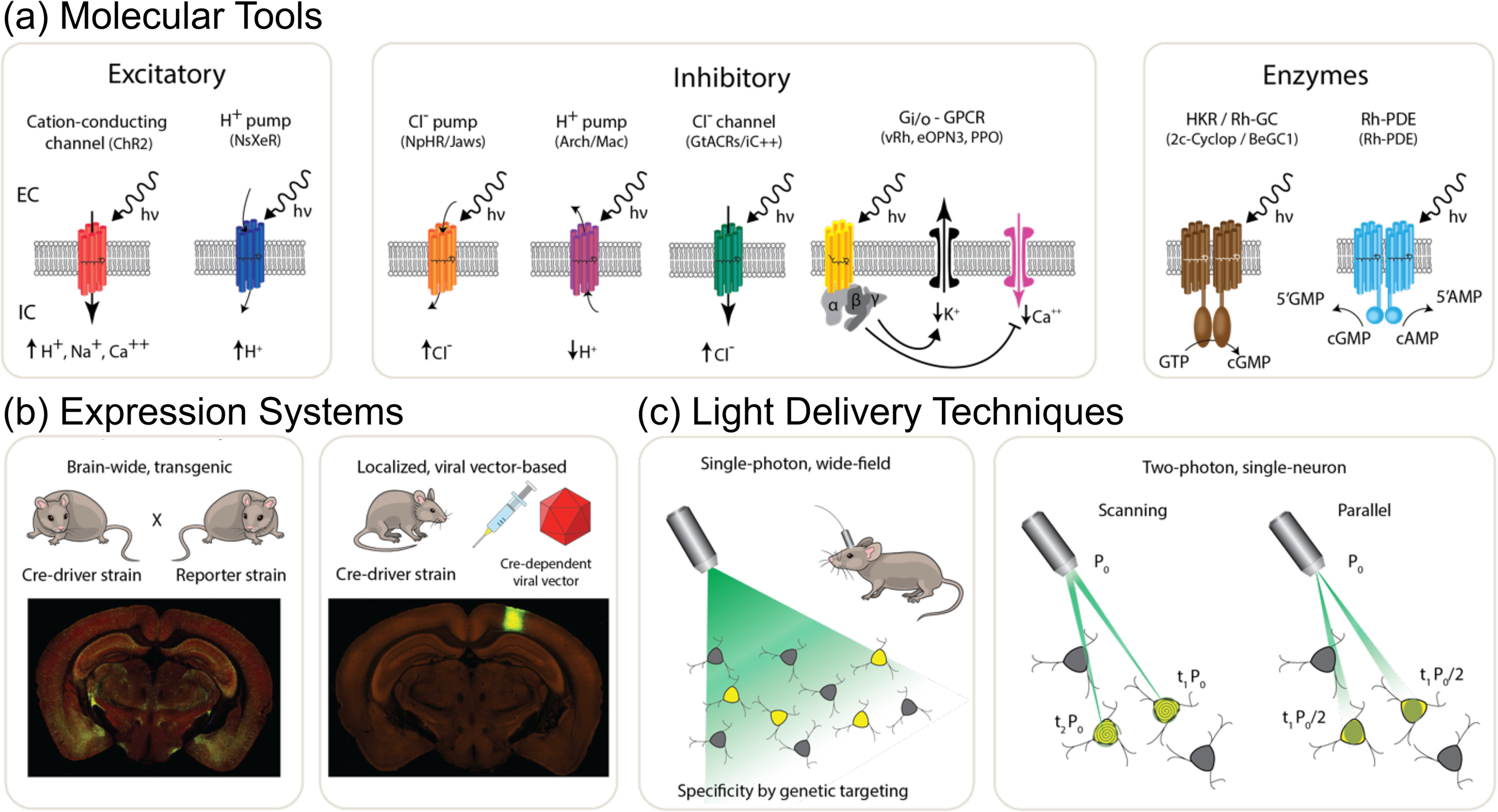
ابزارهای اپتوژنتیک، هدف گذاری ژنتیکی و تکنیک های نوری. (الف) سه دسته اصلی از ابزارهای اپتوژنتیک مبتنی بر رودوپسین: پمپ ها و کانال های تحریکی (سمت چپ). اپسین های بازدارنده متشکل از کانال رودوپسین های رسانای کلرید، پمپ های پروتون و کلرید، و رودوپسین های جفت شده با پروتئین G همراه با مسیر بازدارنده Gi/o (مرکز). آنزیم رودوپسین (راست)؛ گروه هیستیدین کیناز و گروه فسفودی استراز نشان داده شده است. (ب) سیستمهای بیان: دو نمونه از تکنیکهای تحویل ژن که برای بیان ابزارهای اپتوژنتیک در جمعیتهای نورون هدف استفاده میشوند: عبور از خط موش محرک recombinase با دیگری که یک محرک اپتوژنتیک وابسته به recombinase را بیان میکند (سمت چپ) یا تزریق استریوتاکتیک یک ناقل ویروسی که محرک اپتوژنتیک (ج) تکنیکهای تحویل نور برای اپتوژنتیک: (سمت چپ) روشنایی میدان وسیع نورونها که یک محرک اپتوژنتیک را از طریق فیبر نوری چند حالته کاشته شده مزمن نشان میدهند یا (راست) روشنایی 2P تک تک نورونها با استفاده از اسکن مارپیچی یک نقطه محدود پراش یا موازی. نورپردازی اشکال توسعه یافته با استفاده از رویکردهای شکل دهی جبهه موج. تصاویر پانل (ب) از موسسه آلن برای علوم مغز هستند
محرک های اپتوژنتیک
تکنیکهای اپتوژنتیک علوم اعصاب را در دهه گذشته متحول کرده است و ابزار بیسابقهای برای دستکاری مدارهای عصبی با نور ارائه میدهد. 130 با هدف درک سازمان و عملکرد مغز، اپتوژنتیک با کشف کانالهای کاتیون رساننده نوری ChR1 آغاز شد. و ChR2291292 و استفاده از ChR2 برای برانگیختن نورونهای پستانداران. ابزارهایی برای فعال سازی و خاموش کردن فعالیت های عصبی، برای مدولاسیون مسیرهای سیگنالینگ پروتئین G و برای مدولاسیون مستقیم مسیرهای پیام رسان دوم [شکل. 17 (الف)]. ابزارهای اپتوژنتیک نیز برای کنترل مبتنی بر نور بر بیان ژن، آزادسازی سیناپسی و مسیرهای سیگنالینگ بیوشیمیایی توسعه یافته اند. در حالی که این موارد اخیراً در جاهای دیگر مورد بررسی قرار گرفته اند، 297-301 ما در اینجا بر رایج ترین ابزارهای کاربردی که بر اساس پروتئین رودوپسین میکروبی و مهره داران هستند تمرکز خواهیم کرد. مشترک همه این ابزارهای جدید، استفاده از پروتئین های طبیعی حساس به نور به عنوان محرک برای هدایت فرآیندهای سلولی است. پیشرفت حیاتی و جذابیت اصلی ابزارهای اپتوژنتیک برای تحقیقات علوم اعصاب این است که این ابزارها همگی از نظر ژنتیکی رمزگذاری شده اند. این امکان استفاده از تکنیکهای مهندسی ژنتیک را برای هدایت بیان ابزارهای اپتوژنتیک به جمعیتهای سلولی دقیقاً تعریفشده، از طریق اجرای تکنیکهای تراریخته و/یا فناوری ناقل ویروسی فراهم میکند. 17 (ب)]. انتخابپذیری از طریق توالیهای پروموتر یا تقویتکننده خاصی که منحصراً در جمعیتهای سلولی هدف بیان میشوند، به دست میآید. سلولهایی که پروتئین حساس به نور را بیان میکنند به روشی به نور پاسخ میدهند که با ویژگیهای پروتئین خاص مورد استفاده تعریف شده است، در حالی که همسایههای غیر بیانگر آنها بدون تغییر باقی میمانند. با هم، تلاقی ویژگی های ژنتیکی و عدم حساسیت طبیعی اکثر عناصر بافت مغز به نور، اپتوژنتیک را به یک تکنیک قدرتمند برای تشریح عملکردی مدارهای مغز در حیوانات زنده تبدیل می کند. اپتوژنتیک برای طیف وسیعی از اهداف تجربی استفاده شده است، از تشریح عملکردی اتصالات مدار عصبی302 تا بررسی سهم جمعیت های عصبی تعریف شده به رفتارهای بسیار خاص303 تا توسعه مداخلات نور محور در مدل های حیوانی اختلالات عصبی304 و اخیراً ، درمان بیماران انسانی مبتلا به بیماری نورودژنراتیو.305