Sepanta Laser Spadan
شرکت سپنتا لیزر اسپادان سهامی خاص
Sepanta Laser Spadan
شرکت سپنتا لیزر اسپادان سهامی خاصحسگر نوری
تکنیکهای نوری مانند تصویربرداری فلورسانس، اصلیترین ابزار برای بررسی برهمکنشهای مولکولی زیستی هم در داخل بدن و هم در شرایط آزمایشگاهی بوده است. اخیراً چندین تکنیک نوری بدون برچسب، یعنی آنهایی که نیازی به برچسب زدن مولکول مورد نظر ندارند، به عنوان مثال، با فلوروفور توسعه یافته است. به عنوان مثال می توان به تکنیک های مبتنی بر اثر رامان (SERS) و سنجش تداخل پراشی اشاره کرد.
کاوشگرهای ملایم برای فیزیولوژی 4 بعدی
کاوشگرهای ملایم برای فیزیولوژی 4 بعدی
میزبان: گروه فنی پروب های مولکولی و نانوبیو اپتیک
تصویربرداری فراطیفی پزشکی: یک بررسی
خلاصه
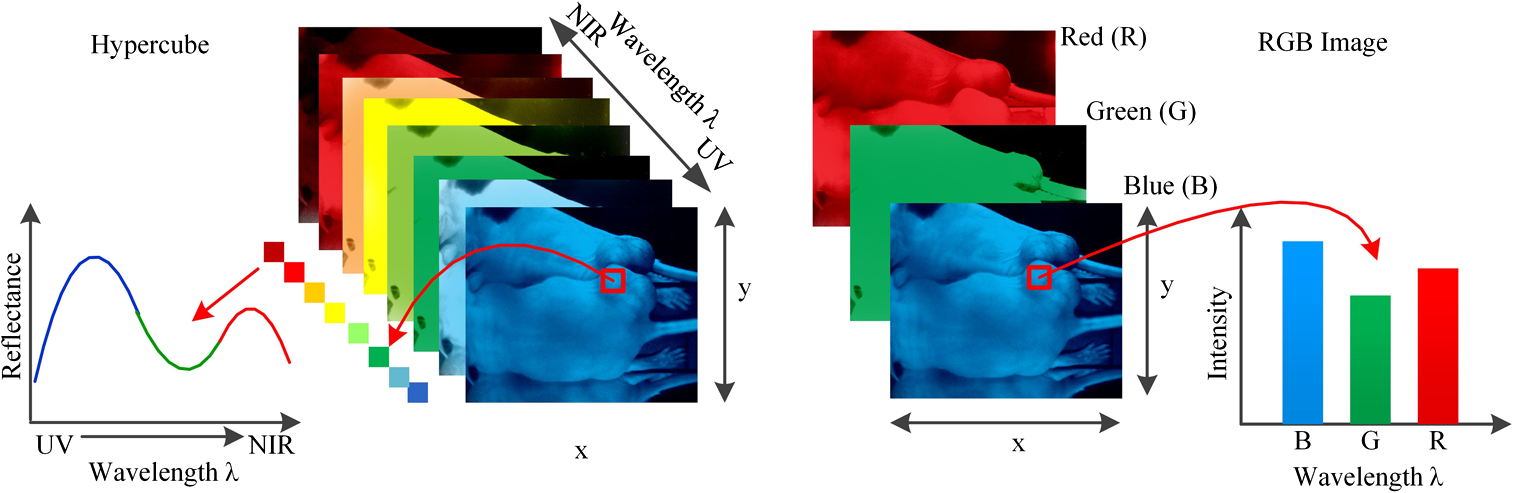
تصویربرداری فراطیفی (HSI) یک روش تصویربرداری نوظهور برای کاربردهای پزشکی، به ویژه در تشخیص بیماری و جراحی با هدایت تصویر است. HSI یک مجموعه داده سه بعدی به نام hypercube با دو بعد فضایی و یک بعد طیفی به دست می آورد. تصویربرداری طیفی با تفکیک فضایی بدست آمده توسط HSI اطلاعات تشخیصی در مورد فیزیولوژی، مورفولوژی و ترکیب بافت ارائه می دهد. این مقاله مروری مروری بر ادبیات فناوری تصویربرداری فراطیفی پزشکی و کاربردهای آن ارائه میکند. هدف این نظرسنجی سه چیز است: معرفی برای کسانی که تازه وارد این رشته شده اند، یک مرور کلی برای کسانی که در این زمینه کار می کنند، و مرجعی برای کسانی که در جستجوی ادبیات در یک برنامه خاص هستند.
1. معرفی
تصویربرداری فراطیفی (HSI) که طیفسنج تصویربرداری نیز نامیده میشود، از سنجش از دور منشا گرفته و برای کاربردهای مختلف توسط ناسا مورد بررسی قرار گرفته است. مناطقی از جمله باستان شناسی و حفاظت از هنر، 3،4 کنترل پوشش گیاهی و منابع آب، 5،6 کنترل کیفیت و ایمنی غذا، 7،8 پزشکی قانونی، 9،10 تشخیص صحنه جرم، 11،12 زیست پزشکی، 13،14 و غیره.
به عنوان یک روش تصویربرداری نوظهور برای کاربردهای پزشکی، HSI پتانسیل زیادی برای تشخیص بیماری های غیرتهاجمی و راهنمایی های جراحی ارائه می دهد. نور تحویلی به بافت بیولوژیکی تحت پراکندگی های متعدد ناشی از ناهمگنی ساختارهای بیولوژیکی و جذب عمدتاً در هموگلوبین، ملانین و آب در حین انتشار در بافت قرار می گیرد. فرض بر این است که ویژگی های جذب، فلورسانس و پراکندگی بافت در طول دوره تغییر می کند. پیشرفت بیماری.17 بنابراین، نور منعکس شده، فلورسنت، و عبوری از بافت گرفته شده توسط HSI حاوی اطلاعات کمی تشخیصی در مورد آسیب شناسی بافت است.17-20 در سال های اخیر، پیشرفت در دوربین های ابرطیفی، روش های تجزیه و تحلیل تصویر، و قدرت محاسباتی این امکان را فراهم کرده است. برای بسیاری از کاربردهای هیجان انگیز در زمینه پزشکی.
در ادامه، هدف ما معرفی و توضیح فناوری تصویربرداری فراطیفی پزشکی (MHSI) و ارائه مروری بر ادبیات سخت افزار، نرم افزار و برنامه های کاربردی MHSI است. این نظرسنجی ادبیاتی را از پاییز 1988 تا بهار 2013 پوشش میدهد. ما از اصول اولیه با مکانیسمهای HSI و وضعیت توسعه فعلی آن شروع میکنیم. سپس MHSI را بر اساس حالت اکتساب، محدوده طیفی و وضوح فضایی، حالت اندازهگیری، دستگاههای پراکنده، آرایههای آشکارساز و ترکیب با تکنیکهای دیگر طبقهبندی میکنیم. روش های تجزیه و تحلیل تصویر برای MHSI با تأکید بر پیش پردازش، استخراج و انتخاب ویژگی، و روش های طبقه بندی خلاصه می شود. بخش کاربردها به ادبیات موجود در مورد تشخیص بیماری و راهنمایی جراحی اشاره دارد. این کاربردها عمدتاً نواحی فرابنفش (UV)، مرئی (VIS) و نزدیک مادون قرمز (نزدیک به IR یا NIR) را پوشش می دهند. خوانندگان علاقه مند می توانند برای کاربردهای بیشتر در مناطق مادون قرمز میانی (IR یا MIR) به مقالات بررسی دیگر مراجعه کنند. در نهایت، ما با بحث در مورد دستاوردهای سال های گذشته و برخی از چالش های آینده به پایان می رسیم.
2. اپتیک بافت
انتشار نور در بافت یک مشکل مهم در کاربردهای پزشکی و توسعه روشهای تشخیصی است. بنابراین، این بخش به بررسی مختصری از مکانیسم های تعامل بافت نور، فرآیندهای نوری درگیر در HSI و اطلاعات تشخیصی مفید ارائه شده توسط HSI اختصاص دارد.
نوری که وارد بافت بیولوژیکی میشود، در حین انتشار در بافت، تحت چندین رویداد پراکندگی و جذب قرار میگیرد. 23 بافتهای بیولوژیکی از نظر ترکیب ناهمگن با تغییرات مکانی در خواص نوری هستند. پراکندگی های مهم اندامک های درون سلولی هستند که اندازه آنها از آنها شروع می شود
<
100
نانومتر
تا 6 میکرومتر به عنوان مثال، میتوکندری ها پراکنده غالب در بین اندامک ها هستند. ساختار یک غشای لیپیدی و چینهای لیپیدی که در داخل آن قرار دارند، به میتوکندری کنتراست نوری بالایی با سیتوپلاسم اطراف میدهد و اثرات پراکندگی قوی مشاهده شده را ایجاد میکند. شکل و اندازه سلولها در انواع مختلف بافت با ابعاد چند میکرون و بزرگتر متفاوت است. خواص پراکندگی بافتهای پشتیبان متشکل از سلولها و پروتئینهای خارج سلولی (الاستین و کلاژن و غیره) ناشی از ناهمگونیهای کوچک مقیاس است. و تغییرات در مقیاس بزرگ در ساختارهایی که آنها تشکیل می دهند.
عمق نفوذ نور به بافت های بیولوژیکی بستگی به این دارد که بافت چقدر نور را جذب می کند. اکثر بافت ها به اندازه کافی جاذب های ضعیفی دارند که اجازه نفوذ نور قابل توجهی را در پنجره درمانی می دهند، از 600 تا 1300 نانومتر.24 در پنجره درمانی، پراکندگی بیش از حد جذب می شود، بنابراین نور منتشر شده منتشر می شود. جذب بافت تابعی از ترکیب مولکولی است. مولکول ها فوتون ها را جذب می کنند
نور فرود میتواند مستقیماً روی سطح بافت منعکس شود یا به دلیل تغییرات فضایی تصادفی در چگالی بافت (غشاها، هستهها و غیره) پراکنده شود و سپس به سطح بافت منتقل شود.27 نور به دلیل پراکندگی چندگانه در جهت تصادفی میشود. و این به عنوان بازتاب منتشر شناخته می شود که اطلاعاتی در مورد پراکندگی و جذب اجزا در اعماق بافت ارائه می دهد. خواص بیش از حجم معینی از بافت. 31 آگاهی از منشاء سیگنال های پراکندگی و جذب، مدل سازی و تفسیر دقیق داده های بازتاب را تسهیل می کند. سیگنال بازتاب اندازه گیری شده از بافت اپیتلیال توسط خواص ساختاری و بیوشیمیایی بافت تعیین می شود. تغییرات در مورفولوژی بافت، از جمله هیپرپلازی، ازدحام هسته، تخریب کلاژن در ماتریکس خارج سلولی توسط متالوپروتئینازهای ماتریکس، و افزایش نسبت هسته به سیتوپلاسمی، که با پیشرفت بیماری، می تواند بر سیگنال های پراکنده تأثیر بگذارد. با پیشرفت بیماری، جذب هموگلوبین ممکن است تحت تأثیر رگزایی و هیپوکسی بافتی و غیره قرار گیرد. بنابراین، تغییرات در حالات بیماری باید به تغییرات متناظر در الگوهای نور منعکس شده از بافت منجر شود.
تصویربرداری بازتابی میتواند تغییرات موضعی در خواص پراکندگی و جذب بافت را تشخیص دهد و تصویربرداری فلورسانس میتواند تغییرات در ترکیب بیوشیمیایی بافت را با آشکار کردن سطوح فلوروفورهای درونزا بررسی کند. علاوه بر این، سیستم HSI را می توان با سایر تکنیک های موجود، مانند میکروسکوپ و کولپوسکوپ، تطبیق داد تا اطلاعات تکمیلی را به شیوه ای دقیق تر و قابل اعتمادتر ارائه دهد. میکروسکوپ انتقال HSI یکی از نمونه های این فناوری های ترکیبی است و در آسیب شناسی بافت مورد استفاده قرار گرفته است.
تصویربرداری جراحی و بیوفوتونیک
علایق تحقیقاتی حول توسعه و کاربرد فناوری فوتونیک با آندوسکوپی برای کاربردهای تصویربرداری جراحی، از جمله تصویربرداری چند طیفی، تصویربرداری با تفکیک قطبی، تصویربرداری فلورسانس، و استفاده از نانومیلههای طلا با برچسب فلورسنت برای ترانوستیک است. پروژههای بیشتر شامل کار بر روی توسعه سیستمهای روشنایی و بینایی برای آندوسکوپی است که منابع نور مینیاتوری مانند LED و دیودهای لیزر را با تکنیکهای بینایی کامپیوتری برای روشنایی ساختاریافته و بازسازی سطح بافت و همچنین استفاده از هدایت روباتیک پروبهای نوری ترکیب میکند. این دستگاه ها در جراحی های کم تهاجمی و توسعه سیستم های جدید جراحی رباتیک کمکی انعطاف پذیر کاربرد پیدا می کنند.
نور ساختاری و تصویربرداری فلورسانس تحریک دو فوتون
"تصویربرداری با کنتراست بالا از طریق اسپری های نوری متراکم با استفاده از نور ساختاری و تصویربرداری فلورسانس تحریک دو فوتون"
تصویربرداری و مشخص کردن اسپری های اتمیزه کننده به دلیل پراکندگی نور متعددی که توسط قطرات اطراف ایجاد می شود بسیار چالش برانگیز است. این موضوع امکان تجزیه و تحلیل پدیده های تجزیه مایع و تشکیل قطرات را در چنین محیط های پراکندگی محدود کرده است. در طول دهه گذشته، ما در حال توسعه انواع تکنیکهای تصویربرداری جدید بودهایم که امکان کاهش و سرکوب تاری تصویر را فراهم میکند و منجر به تجسم کنتراست بالا اسپریهای متراکم نوری میشود. این رویکردهای تجربی مبتنی بر استفاده از روشهای روشنایی ساختاریافته و همچنین تصویربرداری فلورسانس تحریک دو فوتونی هستند. در نهایت، شبیهسازیهای عددی مبتنی بر شبیهسازی مونت کارلو شتابدار GPU نیز برای درک بیشتر اثرات ناشی از پراکندگی نور چندگانه و بهینهسازی استراتژیهای فیلتر نوری پیشنهادی انجام شدهاند.
به استخوان: نقشه برداری سه بعدی از الگوهای معدنی در داخل مرکز مهره کوسه
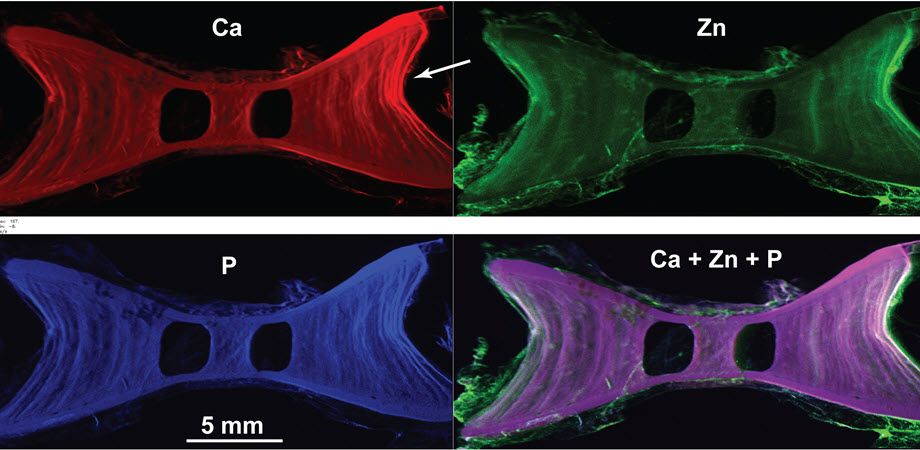
به استخوان: نقشه برداری سه بعدی از الگوهای معدنی در داخل مرکز مهره کوسه
محققان سازماندهی مولکولی بافت استخوانی معدنی را در کوسه ها بررسی می کنند
کوسه ها که در آب های عمیق و کم عمق در سراسر اقیانوس ها یافت می شوند، برخی از قدیمی ترین موجودات زنده سیاره زمین هستند. اسکلت های کوسه، ساخته شده از بافت لاستیکی به نام غضروف، دانشمندان را برای قرن ها مجذوب خود کرده است. کوسه ها با سرعت زیاد زیر آب های عمیق شنا می کنند و اسکلت آنها فشار و فشار زیادی را تجربه می کند. این بارهای ناشی از شنا توسط مرکز - بافت استخوانی معدنی موجود در مهرههای کوسه تحمل میشود. با این حال، از نقطه نظر عملکردی، کاملاً مشخص نیست که ساختارهای معدنی سه بعدی پیچیده مرکز کوسه چگونه بارها را در آن پشتیبانی و توزیع می کنند.
برای به دست آوردن بینش بیشتر در مورد ویژگی های خاص مرکز کوسه، یک تیم بین رشته ای از محققان از رویکرد جدیدی استفاده کردند که در آن پراش پراکنده انرژی (EDD) با استفاده از تابش سنکروترون ایکس چند رنگی انجام شد. یافته های آنها در مقاله جدیدی که در مجله SPIE's Journal of Medical Imaging (JMI) منتشر شده گزارش شده است. استوارت آر، نویسنده مسئول توضیح می دهد: "مطالعاتی که از پراش سه بعدی برای نقشه برداری بافت معدنی استفاده می کنند، بسیار نادر هستند، و چنین مطالعات پراشی بر روی بافت های مرکز کوسه انجام نشده است. اطلاعاتی که می توانیم از روش های سنتی جذب یا تصویربرداری کنتراست فاز به دست آوریم، بسیار محدود است." سهام دانشکده پزشکی Feinberg دانشگاه نورث ایسترن. "خواص مکانیکی بافت های معدنی شده به شدت به نحوه جهت گیری کانی بستگی دارد، و ما می خواستیم از تکنیک جدید خود برای به دست آوردن نقشه های 3 بعدی EDD آموزنده از توزیع جهت گیری های نانوبلورهای زیست آپاتیت در بافت معدنی کوسه های آبی استفاده کنیم."
برخلاف روشهای متداول پراش اشعه ایکس که از پرتوهای یک انرژی استفاده میکنند، EDD با پرتوهای ایکس با طولموجهای مختلف تابش میکند. نانوکریستالهایی که جهتگیریهای متفاوت دارند، طولموجهای مختلف را پراش میکنند، بنابراین حرکت نمونه در طول پرتو اجازه میدهد تا جهتگیریهای کریستالی متنوع را ترسیم کنند. این تیم تکنیک پراش را با توموگرافی ریز کامپیوتری و نقشه برداری فلورسانس ترکیب کردند تا اطلاعات تکمیلی را اضافه کنند. این تکنیک ترکیبی به طور موثر به محققان این امکان را داد که «داخل» بافت مرکز را در سطح مولکولی ببینند و نقشههای سه بعدی با وضوح بالا از آرایش بیوآپاتیت در آن بسازند.
ساختار اصلی مرکز کوسه آبی دیواره های مخروطی و گوه ها هستند. محققان دریافتند که جهتگیری بیوآپاتیت بین دیوارههای مخروطی و گوهها متفاوت است و این موضوع را به این شکل تفسیر کردند که به مهرههای کوسه اجازه میدهد به ترتیب در برابر انحرافات جانبی و محوری در طول شنا مقاومت کنند. این یافتهها بینشهای جالبی را در مورد رابطه ساختار-عملکرد اسکلت کوسه ارائه میدهد و شاید بتوان آن را برای ساختارها و بافتهای استخوانی موجودات دیگر به کار برد.
به گفته برت مولر، دانشکده پزشکی دانشگاه بازل و ویرایشگر مهمان JMI، "ترکیب پراش و توموگرافی با داده های تصویربرداری فلورسانس، بینش دقیقی از سازمان کریستالی استخوان و غضروف تا سطح مولکولی ارائه می دهد. نقطه شروعی را ارائه می دهد. برای درک عمیق ساختارهای جهت دار منحصر به فرد در بافت های استخوانی و عملکرد اسکلتی مرتبط."
با نشان دادن اینکه نمونههای بافت معدنی را میتوان بهصورت سه بعدی با استفاده از توموگرافی EDD ترسیم کرد، این مطالعه اثبات مفهومی را ارائه میکند که پیامدهای مهمی برای مطالعه استخوانهای جسد انسان و حیوان در علوم پزشکی دارد. استوک میگوید: «نقشهبرداری سهبعدی با EDD میتواند به ما در درک تفاوتهای نانوسکوپی در ساختار معدنی بین استخوانهای سالم و بیمار، مانند پوکی استخوان، کمک کند و همچنین بفهمیم که چگونه استخوانهای بهبود یافته با استخوانهای بومی متفاوت هستند. چنین مطالعاتی میتواند منجر به پیشرفتهای بالینی قابل توجهی شود.»
در حالی که توموگرافی سه بعدی EDD ممکن است نتواند به تمام سوالات ما در مورد استخوان ها پاسخ دهد، مطمئناً می تواند اطلاعات کلیدی را ارائه دهد و راه را برای پیشرفت های بیشتر هموار کند. هیچ استخوانی در مورد آن درست نکنید.
روش های تصویربرداری برای نظارت بر اثرات حاد درمانی پس از فوتوایمونوتراپی نزدیک به مادون قرمز در داخل بدن
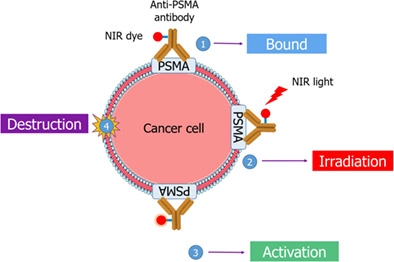
فوتوایمونوتراپی مادون قرمز نزدیک (NIR-PIT) باعث مرگ سلولی فوری پس از تابش نور مادون قرمز نزدیک (NIR) می شود. اثرات درمانی حاد ناشی از NIR-PIT قبل از تغییر اندازه تومور ضروری است که با روش های تصویربرداری نظارت شود. ما روشهای تصویربرداری، از جمله تصویربرداری فلورسانس و طول عمر فلورسانس، تصویربرداری تشدید مغناطیسی، توموگرافی انتشار پوزیترون 18F-fluorodeoxyglucose، توموگرافی انسجام نوری را برای ارزیابی اثرات درمانی حاد پس از NIR-PIT، خلاصه و مقایسه کردیم، و هدف آن ارائه یک مزیت و مزیت بود. معایب هر روش برای ارزیابی در کاربردهای بالینی
توموگرافی نوری و طیف سنجی
توموگرافی نوری و طیف سنجی
اپتیک پراکنده (DOT/DOS، DCT/DCS)
پوشش تمام جنبه های برجسته اعم از الگوریتم ها و دستگاه ها تا کاربردهای پیش بالینی و بالینی.
تصویربرداری لکه های لیزری
به طور کلی، این منطقه استفاده از لکه های لیزری و آمار آنها را برای تصویربرداری و نظارت زیست پزشکی پوشش می دهد.
توموگرافی فوتو آکوستیک و طیف سنجی
پوشش تمام جنبه های برجسته اعم از الگوریتم ها و دستگاه ها تا کاربردهای پیش بالینی و بالینی.
طیف سنجی رامان و تصویربرداری فلورسانس
این حوزههای نوظهور در همه سطوح از پایه فیزیکی گرفته تا دستگاههای جدید جدید تا کاربردهای پیش بالینی و بالینی نشان داده شدهاند.
آینده
پیشرفت های تکنولوژیکی جدید برای کاربردهای پیش بالینی و بالینی که طیف وسیعی از روش ها را پوشش می دهد.