Sepanta Laser Spadan
شرکت سپنتا لیزر اسپادان سهامی خاصSepanta Laser Spadan
شرکت سپنتا لیزر اسپادان سهامی خاص"ابزار ساخته شده از نور": برنده جایزه نوبل علم لیزر توضیح داده شده است

جرارد مورو فرانسوی یکی از سه محققی بود که برنده جایزه نوبل فیزیک ۲۰۱۸ برای اختراعات در زمینه فیزیک لیزر شد.
پس از اینکه سه دانشمند روز سه شنبه جایزه نوبل فیزیک را برای اکتشافات پیشگامانه ای که از قدرت لیزر استفاده می کنند، بردند، در اینجا چند واقعیت اساسی در مورد تحقیقات آنها آورده شده است.
لیزر چیست؟
به گفته ایان ماسگریو، رهبر گروه لیزر Vulcan در مرکز لیزر مرکزی بریتانیا، لیزرها درست مانند مشعل ها، اما دارای خواص ویژه هستند.
معمولاً وقتی نور از مشعل خارج میشود، روشن میشود - او آن را با بچههایی مقایسه کرد که در جهات مختلف مدرسه را ترک میکنند و کتهای مختلفی میپوشند.
او گفت، اما یک لیزر نور را متمرکز می کند، گویی همه بچه ها مجبور شده اند با یک یونیفرم یکسان راهپیمایی کنند.
او افزود که این تفاوت ناشی از حفره ای است که برای به دام انداختن و تنظیم نور قبل از تابش آن و همچنین نحوه تولید نور استفاده می شود.
به همین دلیل آکادمی سلطنتی علوم سوئد از برندگان نوبل روز سه شنبه به عنوان «ابزار ساخته شده از نور» استقبال کرد.
به استخوان: نقشه برداری سه بعدی از الگوهای معدنی در داخل مرکز مهره کوسه
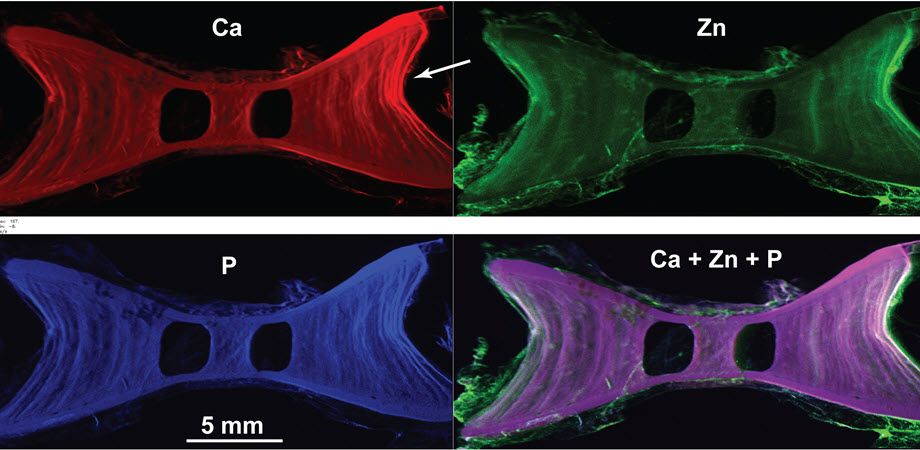
به استخوان: نقشه برداری سه بعدی از الگوهای معدنی در داخل مرکز مهره کوسه
محققان سازماندهی مولکولی بافت استخوانی معدنی را در کوسه ها بررسی می کنند
کوسه ها که در آب های عمیق و کم عمق در سراسر اقیانوس ها یافت می شوند، برخی از قدیمی ترین موجودات زنده سیاره زمین هستند. اسکلت های کوسه، ساخته شده از بافت لاستیکی به نام غضروف، دانشمندان را برای قرن ها مجذوب خود کرده است. کوسه ها با سرعت زیاد زیر آب های عمیق شنا می کنند و اسکلت آنها فشار و فشار زیادی را تجربه می کند. این بارهای ناشی از شنا توسط مرکز - بافت استخوانی معدنی موجود در مهرههای کوسه تحمل میشود. با این حال، از نقطه نظر عملکردی، کاملاً مشخص نیست که ساختارهای معدنی سه بعدی پیچیده مرکز کوسه چگونه بارها را در آن پشتیبانی و توزیع می کنند.
برای به دست آوردن بینش بیشتر در مورد ویژگی های خاص مرکز کوسه، یک تیم بین رشته ای از محققان از رویکرد جدیدی استفاده کردند که در آن پراش پراکنده انرژی (EDD) با استفاده از تابش سنکروترون ایکس چند رنگی انجام شد. یافته های آنها در مقاله جدیدی که در مجله SPIE's Journal of Medical Imaging (JMI) منتشر شده گزارش شده است. استوارت آر، نویسنده مسئول توضیح می دهد: "مطالعاتی که از پراش سه بعدی برای نقشه برداری بافت معدنی استفاده می کنند، بسیار نادر هستند، و چنین مطالعات پراشی بر روی بافت های مرکز کوسه انجام نشده است. اطلاعاتی که می توانیم از روش های سنتی جذب یا تصویربرداری کنتراست فاز به دست آوریم، بسیار محدود است." سهام دانشکده پزشکی Feinberg دانشگاه نورث ایسترن. "خواص مکانیکی بافت های معدنی شده به شدت به نحوه جهت گیری کانی بستگی دارد، و ما می خواستیم از تکنیک جدید خود برای به دست آوردن نقشه های 3 بعدی EDD آموزنده از توزیع جهت گیری های نانوبلورهای زیست آپاتیت در بافت معدنی کوسه های آبی استفاده کنیم."
برخلاف روشهای متداول پراش اشعه ایکس که از پرتوهای یک انرژی استفاده میکنند، EDD با پرتوهای ایکس با طولموجهای مختلف تابش میکند. نانوکریستالهایی که جهتگیریهای متفاوت دارند، طولموجهای مختلف را پراش میکنند، بنابراین حرکت نمونه در طول پرتو اجازه میدهد تا جهتگیریهای کریستالی متنوع را ترسیم کنند. این تیم تکنیک پراش را با توموگرافی ریز کامپیوتری و نقشه برداری فلورسانس ترکیب کردند تا اطلاعات تکمیلی را اضافه کنند. این تکنیک ترکیبی به طور موثر به محققان این امکان را داد که «داخل» بافت مرکز را در سطح مولکولی ببینند و نقشههای سه بعدی با وضوح بالا از آرایش بیوآپاتیت در آن بسازند.
ساختار اصلی مرکز کوسه آبی دیواره های مخروطی و گوه ها هستند. محققان دریافتند که جهتگیری بیوآپاتیت بین دیوارههای مخروطی و گوهها متفاوت است و این موضوع را به این شکل تفسیر کردند که به مهرههای کوسه اجازه میدهد به ترتیب در برابر انحرافات جانبی و محوری در طول شنا مقاومت کنند. این یافتهها بینشهای جالبی را در مورد رابطه ساختار-عملکرد اسکلت کوسه ارائه میدهد و شاید بتوان آن را برای ساختارها و بافتهای استخوانی موجودات دیگر به کار برد.
به گفته برت مولر، دانشکده پزشکی دانشگاه بازل و ویرایشگر مهمان JMI، "ترکیب پراش و توموگرافی با داده های تصویربرداری فلورسانس، بینش دقیقی از سازمان کریستالی استخوان و غضروف تا سطح مولکولی ارائه می دهد. نقطه شروعی را ارائه می دهد. برای درک عمیق ساختارهای جهت دار منحصر به فرد در بافت های استخوانی و عملکرد اسکلتی مرتبط."
با نشان دادن اینکه نمونههای بافت معدنی را میتوان بهصورت سه بعدی با استفاده از توموگرافی EDD ترسیم کرد، این مطالعه اثبات مفهومی را ارائه میکند که پیامدهای مهمی برای مطالعه استخوانهای جسد انسان و حیوان در علوم پزشکی دارد. استوک میگوید: «نقشهبرداری سهبعدی با EDD میتواند به ما در درک تفاوتهای نانوسکوپی در ساختار معدنی بین استخوانهای سالم و بیمار، مانند پوکی استخوان، کمک کند و همچنین بفهمیم که چگونه استخوانهای بهبود یافته با استخوانهای بومی متفاوت هستند. چنین مطالعاتی میتواند منجر به پیشرفتهای بالینی قابل توجهی شود.»
در حالی که توموگرافی سه بعدی EDD ممکن است نتواند به تمام سوالات ما در مورد استخوان ها پاسخ دهد، مطمئناً می تواند اطلاعات کلیدی را ارائه دهد و راه را برای پیشرفت های بیشتر هموار کند. هیچ استخوانی در مورد آن درست نکنید.
زمان کوتاه: تغییرات زمانی برهمکنش نور-ماده باعث افزایش فرامواد فوتونی می شود.

زمان کوتاه: تغییرات زمانی برهمکنش نور-ماده باعث افزایش فرامواد فوتونی می شود.
یک شاخه نوظهور از فوتونیک بر تعاملات نور-ماده در رسانه های متغیر با زمان تمرکز می کند
در سطح مشترک بین دو رسانه، نور تا حدی به سمت عقب به محیطی که از آنجا آمده است منعکس می شود و تا حدودی به محیط مجاور منتقل می شود، مانند پرتو نوری که وارد حوضچه آب می شود. الگوهای موج نوری که از این فرآیندها به وجود میآیند را میتوان با استفاده از فرامواد فوتونیک، که پاسخهای الکترومغناطیسی نوظهوری را ارائه میکنند که اساساً با واکنشهای مواد طبیعی متفاوت است، بهطور مفیدی طراحی کرد.
اما وقتی رابط بین دو ماده را به موقع تغییر دهیم چه اتفاقی میافتد؟ به بیان تصویری، اگر ته استخر به طور ناگهانی بلند یا پایین بیاید، چه؟ در مورد اینکه آیا در یک لحظه خاص از زمان، خواص مادی یک محیط فوراً تغییر می کرد - مثلاً از آب به شراب؟ در فصل مشترک بین دو ماده فوتونیک، تکانه نور حفظ می شود، در حالی که انرژی آن بین امواج الکترومغناطیسی و محیط مبادله می شود. با این حال، رابطه علی بین حادثه و میدان های پراکنده اساساً تغییر می کند: هر دو موج پراکنده در این مورد در محیط اصلاح شده منتشر می شوند.
اگر با زرادخانه پدیده های پراکندگی که در چند دهه گذشته در فیزیک امواج آشکار شده است ترکیب شوند، این تفاوت های اساسی بین پراکندگی مکانی و زمانی می تواند منجر به طیف بسیار گسترده ای از مفاهیم و کاربردهای جدید در فوتونیک و همچنین امواج دیگر از جمله امواج صوتی شود. .
در بررسی منتشر شده در Advanced Photonics، یک تیم بینالمللی مروری جامع از آخرین پیشرفتها در این شاخه جدید و سریع در حال توسعه فوتونیک با تمرکز بر تعاملات نور-ماده در رسانههای متغیر با زمان ارائه میکند. با شروع از بلوک های ساختمانی اصلی پراکندگی زمانی، آنها طیف گسترده ای از فرصت ها را برای دستکاری موج باز شده توسط اشکال مختلف تغییر زمان بررسی می کنند. آنها به فرآیندهای پراکندگی زمانی متعدد نگاه می کنند تا کریستال های زمان فوتونیک دوره ای و شبه تناوبی را همراه با جهت های جدیدی که توسط این سازه ها برای فیزیک توپولوژیک در حوزه زمان باز می شود، بررسی کنند. آنها در مورد مهندسی ابعاد فرکانس مصنوعی، بهره غیر متقابل، و فرمان قدرت، و همچنین سیستمهای متغیر زمان غیر هرمیتی، اختلال زمانی، و دستکاری امواج سطحی قابل دستیابی از طریق مدولاسیون زمانی بحث میکنند.
این بررسی همچنین رسانههای مدولهشده مکانی-زمانی را مورد بررسی قرار میدهد - سیستمهایی که پارامترهای الکترومغناطیسی آنها تحت یک اغتشاش موجمانند سیار قرار میگیرند - که طیف وسیعی از فرصتها را در طرحهای فوتونیک غیرمتقابل به توپولوژیکی، مهندسی اشکال زیر نوری و ابرشورایی حرکت مصنوعی، کشش نوری، کشش نوری و تکجهتای را امکانپذیر میسازد. ، و سایر پدیده های ضد شهودی.
این بررسی با برجسته کردن برخی از امیدوارکنندهترین پلتفرمها برای ترجمه این مفاهیم فوتونیک با زمان متغیر به تحققها و کاربردهای تجربی در فوتونیک به پایان میرسد. آنها همچنین مسیرها و مواد در حال ظهور را برای دستیابی به مدولاسیون زمانی کارآمد، مانند مواد اپسیلون نزدیک به صفر و متاسطحهای دی الکتریک با شاخص بالا، پلاریتون های چاه کوانتومی، مدولاسیون مغناطیسی نوری، فرامواد چند لایه و مواد دو بعدی برجسته می کنند.
اثرات موجی فوتونیک های متغیر با زمان بسیار گسترده است و بدون شک برای سال های آینده طنین انداز خواهد شد.
رویکرد اپتوژنتیک نیازی به استفاده از عینک تشدید کننده ندارد. اعتبار: فناوری های نانوسکوپی
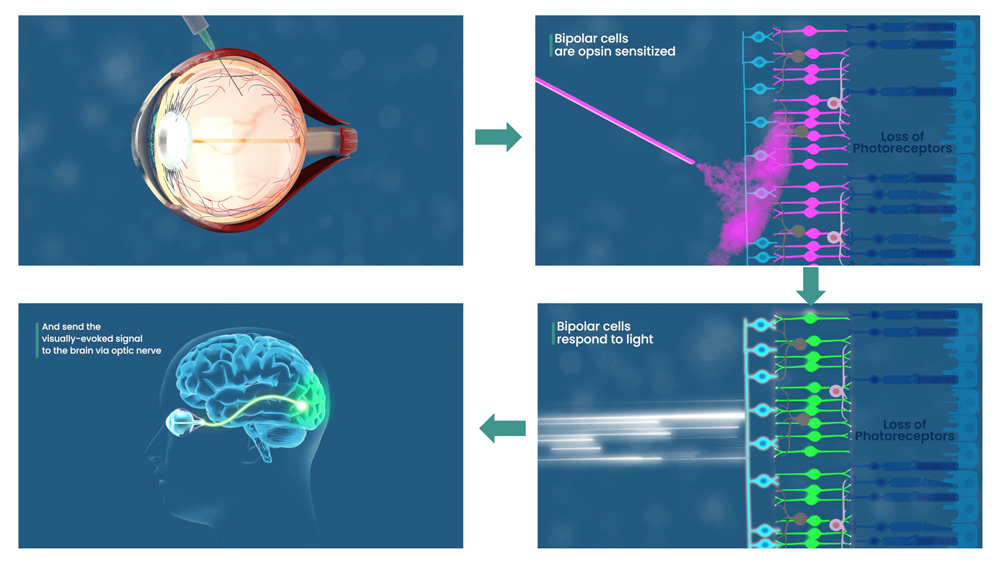
رویکرد اپتوژنتیک نیازی به استفاده از عینک تشدید کننده ندارد. اعتبار: فناوری های نانوسکوپی
بعلاوه، اگر از مواد فتوشیمیایی استفاده می شود، باید رهایش آهسته طولانی مدت را برای به حداقل رساندن فرکانس تزریق نشان دهند. سیستم کلی بازیابی بینایی در صورت اثبات اثر نامطلوب باید قابلیت خاموش شدن را داشته باشد و در حالت ایده آل باید قابل ارتقا باشد. ایساکف اظهار داشت: «فهرست چالش ها دلهره آور است. اما ما داریم به آنجا میرسیم. بسیاری از جعبهها قبلاً بررسی شدهاند و ما مسیری را برای بقیه باز کردهایم.»
بهبود بینایی معنی دار از نظر بالینی
به گفته سامارندرا موهانتی، مانع درمان ترکیبی با استفاده از دستگاههای نوری در کنار اپسین، این است که اطمینان حاصل شود که سمیت نوری در استفاده طولانی مدت محدود است. یک چالش دیگر تطبیق پرتو شبیهسازی پیشبینیشده با سلولهای انتقال یافته با اپسین در شبکیه است که میتوانند تکهای یا در قالب حلقه مرتب شوند. حتی ممکن است سیستم نیاز به ردیابی حرکت چشم داشته باشد و به طور همزمان پرتو اسکن را با توجه به نواحی ترانسدود شده شبکیه تغییر مکان دهد.
در سال 2021، نانوسکوپ نتایج یک کارآزمایی بالینی را منتشر کرد که در آن ژن درمانی اپتوژنتیک این شرکت بینایی معنادار بالینی را به 11 بیمار نابینا شده توسط رتینیت پیگمانتوزا بازگرداند. به گفته این شرکت، این نتایج نشان دهنده اولین بهبود عملکردی معنی دار بالینی است که با درمان اپتوژنتیک به دست آمده است، و انتظار می رود نتایج مثبت بیشتری در پی داشته باشد.
این شرکت در آن زمان خاطرنشان کرد: «ما در یک برنامه توسعه بالینی در مراحل پایانی هستیم، یک کارآزمایی تصادفی دو ماسک چند مرکزی در ایالات متحده، با دادههای بسیار هیجانانگیزی که باید درمان را برای بیماران تسریع کند». ما امیدواریم با Opsin چند مشخصه و پلتفرمهای تحویل ویروسی/غیر ویروسی خود، به جمعیت گستردهای از بیماران مبتلا به شبکیه به شدت تحلیل رفته یا نیمه تحلیل رفته رسیدگی کنیم.
در کنار این پیشرفت در بازگرداندن بینایی به افرادی که آن را از دست دادهاند، اپتوژنتیک همچنین میتواند به بیماران مبتلا به شبکیه نیمه تحلیلرفته نیز رسیدگی کند و با آتروفی جغرافیایی در AMD خشک مقابله کند و در نتیجه به یک بیماری رایج دیگر رسیدگی کند. این امر مستلزم محلی سازی تحویل اپسین به نواحی آتروفیک است.
Mohanty اظهار داشت: "ما یک رویکرد تحویل نوری غیر ویروسی با هدایت OCT ایجاد کردهایم تا ژنهای رمزگذاری کننده اپسین را به مناطق هدف شبکیه ارائه دهیم." این امر التهاب ناشی از استفاده از کپسیدهای ویروسی را از بین میبرد و همچنین به ما اجازه میدهد که سوژه را در همان نواحی آتروفیک تازه تکاملیافته در این بیماریهای پیشرونده دژنراتیو شبکیه دوز مجدد کنیم یا یک اپسین بهبودیافته را تحویل دهیم.»
تیم هیز یک نویسنده مستقل در بریتانیا است. او قبلاً سردبیر صنعت optics.org و مجله Optics & Laser Europe بود. این مقاله در اصل در 2022 SPIE Photonics West Show Daily ظاهر شد.
اپتوژنتیک مسیری امیدوارکننده برای بازیابی بینایی
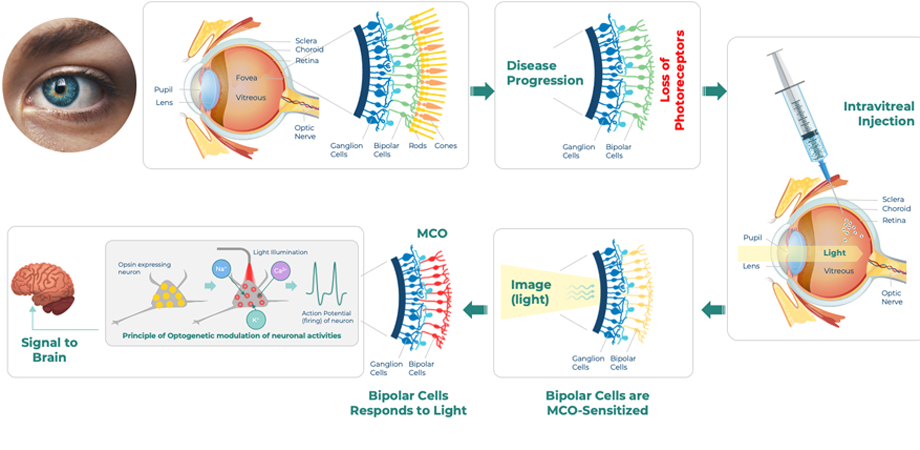
اپتوژنتیک مسیری امیدوارکننده برای بازیابی بینایی
ترجمه با مهندس شکوفه ساتری
درمان اپتوژنتیک MCO نانوسکوپ برای ترمیم بینایی. اعتبار: فناوری های نانوسکوپی.
از دست دادن بینایی می تواند نتیجه بسیاری از شرایط مختلف باشد، به طوری که تصور می شود بیماری ارثی شبکیه شایع ترین علت نابینایی در کشورهای توسعه یافته است. مدیریت تمایل به اقدامات حمایتی به جای درمان دارد، اگرچه روشهای جراحی قابل توجهی با استفاده از انواع مختلف ایمپلنتهای شبکیه نیز توسعه یافتهاند.
اپتوژنتیک، که در آن فعالیت نورون ها یا سلول های دیگر تحت تأثیر نور فرودی قرار می گیرد، می تواند راه حل جذاب تری ارائه دهد. ممکن است بتوان از یک رویکرد اپتوژنتیک برای حساس کردن نورونهای ثانویه و سوم شبکیه چشم به نور استفاده کرد و به آنها اجازه داد بهطور مؤثری جای گیرندههای منحط یا ناکارآمد مسئول از دست دادن بینایی را بگیرند.
این موضوع موضوع جلسه ای در کنفرانس اپتوژنتیک و دستکاری نوری در SPIE Photonics West در ژانویه بود، جایی که سامارندرا موهانتی و تیمی از نانوسکوپ شرکت کنندگان را در مورد آخرین پیشرفت ها در زمینه درمان اختلالات مختلف شبکیه به روز کردند.
موهانتی اظهار داشت: «اپتوژنتیک میتواند نورونهای زندهمانده را حساس به نور کند، تا جایگزین عملکرد حسگر نور گیرندههای غیرفعال شود». "برای اینکه آنها به طور مناسب حساس به نور باشند، به عنوان مثال حساس به محیط باند پهن، به مهندسی مولکولی مناسب به علاوه حساسیت کاوشگر اپتوژنتیک بستگی دارد.
پروتئین opsin که ما استفاده می کنیم و با استفاده از یک ویروس مرتبط با آدنو (AAV) به عنوان ناقل تحویل می شود، باید به اندازه کافی حساس باشد که نورون ها در سطوح کم نور بدون ایجاد سمیت نوری فعال شوند. اپتوژنتیک شامل مولکول های طراحی شده از میکروب ها معمولاً به عنوان یک مهانتی افزود: سیستم تک جزیی، در حالی که انتقال دید طبیعی در انسان شامل تعامل چندین مولکول است، بنابراین سینتیک اپسین باید به اندازه کافی سریع باشد تا امکان پردازش بصری صحنه های متحرک را فراهم کند.
چالش با رویکرد opsin این است که همه ویژگیهای ایدهآل مانند حساسیت بالا، پاسخ طیفی وسیع و پاسخ سریع روشن و خاموش را داشته باشیم که در یک سیستم عملی قابل تشخیص باشند. Nanoscope Technologies اپسینی به نام Multi-Characteristic Opsin توسعه داده است که در آن ساختار منحصر به فرد - یک کانال یونی گذرنده که به یک لیگاند و تقویت کننده متصل شده است - منجر به مکانیسم خاصی از عمل می شود. هدف این است که اجازه دهیم محدوده دینامیکی بازسازی بینایی اپتوژنتیک به چندین مکانیسم مکمل مورد استفاده در چشم طبیعی نزدیک شود.
موهانتی گفت: «مسئله دیگر مربوط به تحویل اپسین به منظور دستیابی به انتقال بالا در سلول های هدف بدون ایجاد التهاب است. موهانتی گفت: "ناقل AAV با دوز بالا ما التهاب محدود و به خوبی کنترل شده را در یک دوره طولانی نشان داده است، در حالی که سایر ناقل های ویروسی در دوز بالا ممکن است منجر به عوارض جانبی طولانی مدت شوند. بنابراین باید به شدت مورد مطالعه و کنترل قرار گیرد."
چالش های در حال رفع شدن
روشهای دیگر برای بازیابی بینایی میتوانند ترکیبی از یک اپسین و یک دستگاه خارجی را به کار گیرند. در حالی که رویکرد اپتوژنتیکی که توسط فناوریهای نانوسکوپ اتخاذ میشود نیازی به استفاده از عینک تقویتکننده ندارد، در عوض از ویژگیهای سفارشی اپسین استفاده میکند، روشهای جایگزین میتوانند از عینک به عنوان بخشی از پلتفرمهای نوری ترکیبی استفاده کنند که برای ثبت یک صحنه خارجی با دوربین و رله در نظر گرفته شده است. آن را به عنوان یک پرتو نور روبشی به شبکیه چشم می رساند. در این رویکردهای درمان ترکیبی، کنترل پالس و شدت نور ارسالی ضروری است، که اغلب از فناوریهای فوتونیک فعلی مانند دستگاههای MEMS، حسگرها و الگوریتمهای پردازش تصویر برای افزایش عملکرد کلی استفاده میکنند.
ایهود ایساکوف از دانشگاه کالیفرنیا، برکلی، که در مورد آن بحث خواهد کرد، اظهار داشت: «برخی از نسخههای این درمانها از عینکهای تشدیدکننده نور استفاده میکنند، و برخی دیگر از عینکهای هوشمند استفاده میکنند که الگوی نور را تغییر میدهند و آن را همانطور که معمولاً در مدار بالادست شبکیه رخ میدهد، تهویه میکنند». استفاده از اپسین میله ای و مخروطی برای ترمیم بینایی اپتوژنتیک در طول کنفرانس.
ما به سیستمی نیاز داریم که به اندازه کافی حساس باشد تا در نور اتاق و روی نمایشگرهای استاندارد رایانه کار کند، سیستمی که دقت بالایی داشته باشد و به اندازه کافی سریع باشد که از تار شدن سوژه یا محیط در حال حرکت جلوگیری کند. و تحویل ژن باید به همان اندازه باشد. ایساکوف گفت: شبکیه تا حد ممکن، در حالی که برای نوع سلولی که به طور متراکم نمایش داده می شود، انتخابی است.
تصویربرداری عملکردی شبکیه چشم انسان با استفاده از تصویربرداری کنتراست لکه ای چندطیفی و لیزری یکپارچه
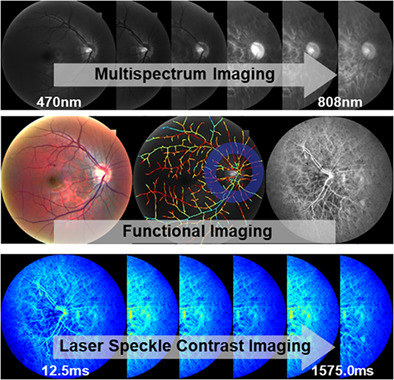
تصویربرداری عملکردی شبکیه چشم انسان با استفاده از تصویربرداری کنتراست لکه ای چندطیفی و لیزری یکپارچه
ترجمه با مهندس شکوفه ساتری
یک ابزار تصویربرداری یکپارچه و مقیاسپذیر شبکیه، ابعاد متعددی از اطلاعات ساختاری و عملکردی شبکیه را در یک گردش کار بالینی سادهشده فراهم میکند، موانع پذیرش بالینی را کاهش میدهد و تحقیقات را با استفاده از این ابزارهای تصویربرداری برای تشخیص، نظارت و روشن کردن پاتوژنز بیماری تسریع میکند.
ادغام جدیدی از تصویربرداری چند طیفی شبکیه (MSI)، اکسیمتری شبکیه و تصویربرداری کنتراست لکه لیزری (LSCI) برای تصویربرداری عملکردی رگهای خونی شبکیه ارائه شده است که به طور بالقوه میتواند به تشخیص زودهنگام یا نظارت بر تغییرات عملکردی اجازه دهد. ما یک ابزار مقرونبهصرفه، مقیاسپذیر و تصویربرداری شبکیه را طراحی و ساختیم که تکنیکهای تصویربرداری ساختاری و عملکردی شبکیه، از جمله MSI، اکسیمتری شبکیه و LSCI را ادغام میکند. تصویربرداری رنگی فوندوس با نوردهی دیود ساطع نور با طول موج 470 نانومتر، 550 نانومتر و 600 نانومتر انجام شد. اکسیمتری شبکیه با استفاده از نور LED 550 نانومتر و 600 نانومتر انجام شد. LSCI جریان خون با استفاده از نور دیود لیزر 850 نانومتری با سرعت 82 فریم در ثانیه انجام شد. LSCI میتواند عروق شبکیه و مشیمیه را بدون نیاز به مواد کنتراست برونزا تجسم کند و میتواند اطلاعات تعیینشده در زمان را در مورد جریان خون ارائه کند، و یک شکل موج پالس قلبی از عروق شبکیه ایجاد کند. این فناوری می تواند به سرعت تصاویر ساختاری MSI، اکسیمتری شبکیه و اطلاعات جریان خون LSCI را در یک جریان کار بالینی ساده بدون نیاز به حرکت بیماران بین ابزارها به دست آورد. نتایج حاصل از روشهای متعدد را میتوان ترکیب و ثبت کرد تا اطلاعات ساختاری و همچنین عملکردی روی شبکیه ارائه شود. این پیشرفتها میتوانند موانع پذیرش بالینی را کاهش دهند، تحقیقات را با استفاده از MSI، اکسیمتری شبکیه و LSCI جریان خون برای تشخیص، نظارت و روشن کردن پاتوژنز بیماری تسریع کنند.
دستکاری چند منظوره گلبول های قرمز با استفاده از موچین های نوری
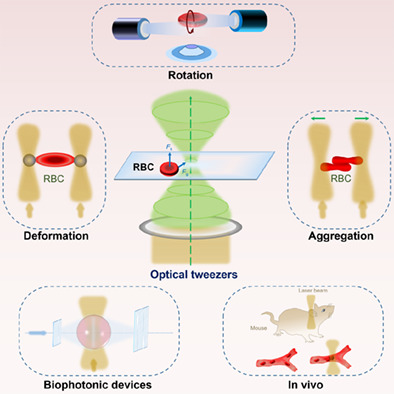
دستکاری چند منظوره گلبول های قرمز با استفاده از موچین های نوری
ترجمه با مهندس شکوفه ساتری
پیشرفتهای اخیر برای استفاده از موچینهای نوری در مطالعات چند منظوره روی گلبولهای قرمز خون (RBC)، از جمله تغییر شکل قابل کنترل، کشش پویا، تجمع گلبولهای قرمز، جداسازی خون، خصوصیات رامان، مونتاژ دستگاههای بیوفوتونیکی و دستکاری درون تنی بررسی شد. با زیست سازگاری بالا و ماهیت غیر تهاجمی، موچین های نوری پتانسیل زیادی برای توصیف عملکردهای فیزیولوژیکی گلبول های قرمز در شرایط آزمایشگاهی و درون تنی از خود نشان داده اند، بنابراین بینش جدیدی برای تشخیص بالینی بیماری های عروقی و تحویل هدفمند نانوپزشکی در داخل بدن ارائه می دهند.


