Sepanta Laser Spadan
شرکت سپنتا لیزر اسپادان سهامی خاص
Sepanta Laser Spadan
شرکت سپنتا لیزر اسپادان سهامی خاصاپتوژنتیک، رمزگذاری ژنتیکی، و کاوشگرهای جدید
اپتیک در مغز انسان
طیفسنجی نزدیک مادون قرمز عملکردی (fNIRS) و توموگرافی نوری منتشر (DOT)
طیف سنجی همبستگی پراکنده.
سیستم های پوشیدنی
رابط های کامپیوتری مغز
تصویربرداری نوری مغز داخل جراحی
پروب های فیبر نوری، طیف سنجی و تصویربرداری آندوسکوپی
مدولاسیون نوری سیستم عصبی مرکزی انسان
عصب شناسی شبکیه
کنتراست لکه ای
مدل سازی عروق و متابولیک
کاربردهای بالینی
عوامل نوری ترجمه (اپتوژنتیک، شاخص های کلسیم، پروب های مولکولی)
لیزرهای فوق سریع برای علوم زیستی - بیوفوتونیک / میکروسکوپ چند فوتونی
لیزرهای فوق سریع برای علوم زیستی - بیوفوتونیک / میکروسکوپ چند فوتونی
شما می توانید از لیزرهای فیبر فوق سریع در بسیاری از کاربردهای علوم زیستی استفاده کنید. به طور کلی یکی از مهمترین کاربردها میکروسکوپ چند فوتونی است. به دلیل طول موج طولانیتر فرآیند چند فوتونی، میتوان به عمق تصویربرداری عمیقتری در مقایسه با میکروسکوپ خطی دست یافت. علاوه بر این، تعامل نور با سلول تنها در فوکوس رخ می دهد که امکان تصویربرداری سه بعدی را فراهم می کند.
لیزرهای سریع برای علوم اعصاب - اپتوژنتیک
لیزرهای سریع برای علوم اعصاب - اپتوژنتیک
اپتوژنتیک یک رشته بسیار جدید از بیوفوتونیک است. ایده استفاده از نور برای فعال کردن یا مهار سیگنالدهی نورونها برای مطالعه شبکه عصبی مغز است. به طور کلی برای آزمایشات در اپتوژنتیک از مراحل مختلفی استفاده می شود.
لیزر برای علوم اعصاب
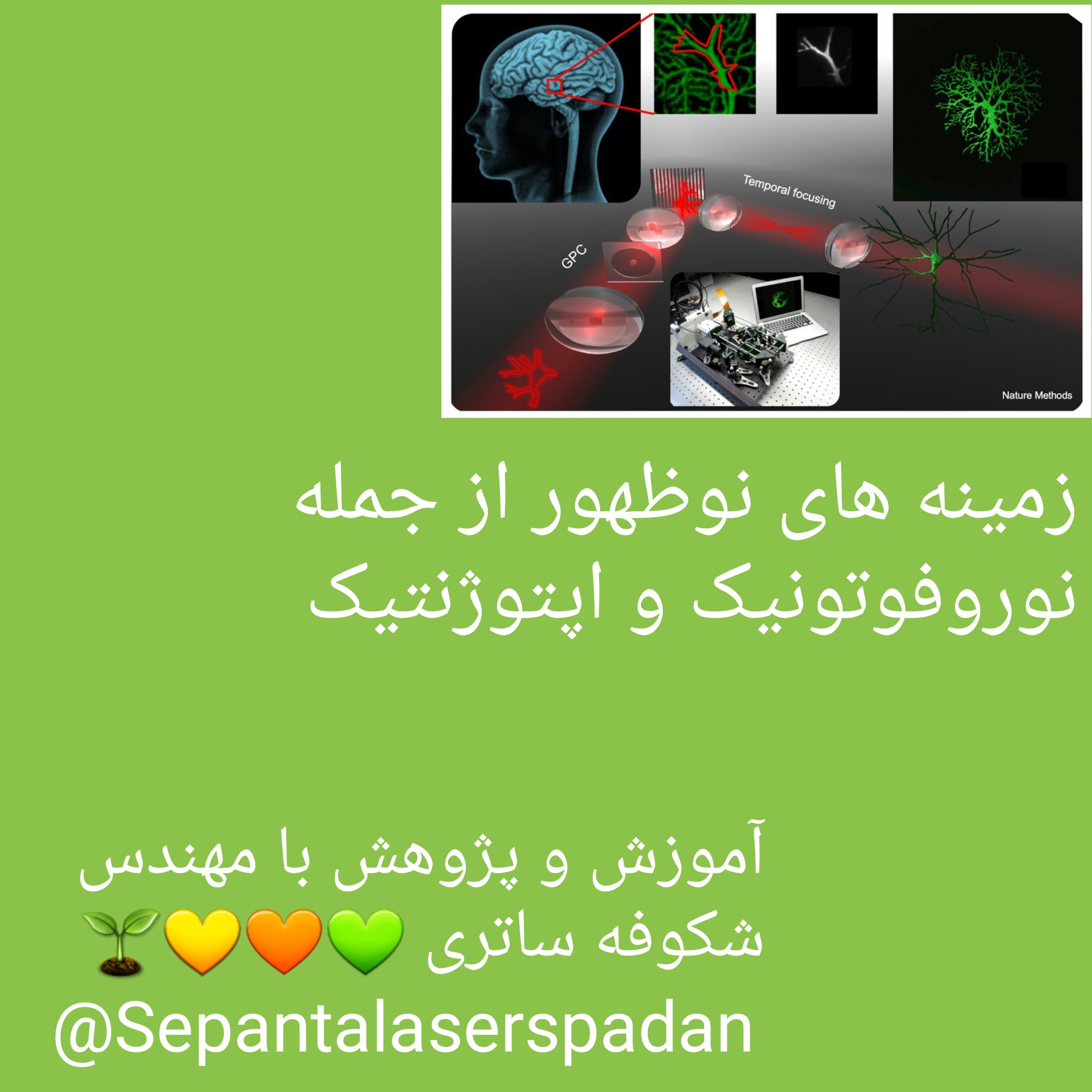
میکروسکوپ فلورسانس 2 فوتونی به یک فناوری کلیدی در تصویربرداری بیولوژیکی در علوم اعصاب تبدیل شده است که امکان مطالعات سه بعدی و غیرتهاجمی ساختار و فعالیت عصبی در مقیاس زیر میکرونی را فراهم می کند. مکانیسم کنتراست در میکروسکوپ 2 فوتونی در تحقیقات عصبشناسی مبتنی بر تحریک پروتئینهای فلورسنت سبز یا قرمز، به اصطلاح GFPs و RFP، توسط دو فوتون در محدوده طیفی مادون قرمز است. برای هدایت این فرآیند غیرخطی و شناسایی نورونها در اعماق مغز زنده، لیزرهای فمتوثانیه با شکل پالس زمانی تمیز و متوسط توان خروجی 1 وات یک پیش نیاز ضروری است. فراتر از تصویربرداری خالص، بازجویی تمام نوری یک رویکرد جدید برای درک چگونگی رفتار الگوهای فعال در فعالیت عصبی است. در چنین آزمایشهایی، تجسم فعالیت عصبی توسط تصویربرداری 2 فوتونی با اپتوژنتیک 2 فوتونی ترکیب میشود تا نورونهای فردی را با فعالسازی نوری کانالهای رودوپسینها در سلول تحریک کنند. با نیاز به هیجان انگیز کردن بسیاری از نورون ها به صورت موازی، نیازهای لیزر و فناوری میکروسکوپ برای اپتوژنتیک 2 فوتونی اساساً با تصویربرداری 2 فوتون متفاوت است. به طور معمول، لیزرهای پرقدرت چند وات در 1030 - 1040 نانومتر با نرخ تکرار در محدوده 100 کیلوهرتز - 1 مگاهرتز در ترکیب با یک مدولاتور نور فضایی (SLM) برای تحریک 10 ثانیه تا 100 ثانیه نورون به طور همزمان استفاده میشوند. برای حمایت و هدایت تحقیقات در علوم اعصاب، TOPTICA مفتخر است مجموعه لیزری خود را برای تصویربرداری 2 فوتونی از GFP ها و RFP ها، FemtoFiber ultra 920 و FemtoFiber ultra 1050، و برای اپتوژنتیک 2 فوتونی کانال های رودوپسین FemtoFiber vario ما را معرفی کند.
نوروفوتونیک، جراحی اعصاب و اپتوژنتیک
نوروفوتونیک، جراحی اعصاب و اپتوژنتیک. در این جلسه موضوعاتی مانند نوروفوتونیک بالینی و ترجمه، تصویربرداری و سنجش عصبی و اپتوژنتیک و دستکاری نوری ارائه می شود.
هدف گیری نوری سلول های سرطانی، بافت سالم را بدون آسیب می گذارد
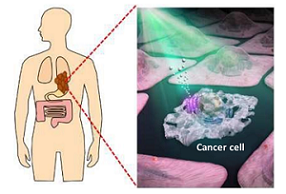
یک گروه تحقیقاتی در دانشگاه اوکایاما در حال کار بر روی روشی برای جلوگیری از آسیب سلول های سالم در طول درمان سرطان هستند. این گروه در حال توسعه یک روش القای نور برای تحریک آپوپتوز سلولی تنها در سلولهای هدف هستند، با استفاده از پروتئین فعال شده با نور به جای مواد شیمیایی.
در حالی که دارو درمانی به عنوان ابزار اصلی درمان سرطان باقی می ماند، بسیاری از داروها یک مشکل مشترک دارند: آنها نه تنها بر روی سلول های سرطانی، بلکه روی سلول های سالم اطراف نیز اثر می گذارند و باعث واکنش های نامطلوب ناخواسته می شوند.
چندین روش درمانی وجود دارد که از نور برای از بین بردن سرطان استفاده می کنند. به عنوان مثال، فوتوایمونوتراپی یک فرم مولکولی هدفمند از فتوتراپی است که درمان فتودینامیک تومور را با ایمونوتراپی ترکیب می کند تا سلول های سرطانی را از بین ببرد.
پروفسور یوکی سودو گفت: "این روش ها از مواد شیمیایی استفاده می کنند و با تکیه بر آنزیم های فعال یا گرما باعث نکروز فیزیکی می شوند." بنابراین، ما نمیتوانیم واکنشهای نامطلوب را هر چقدر هم که آنها را بهبود بخشیم، حذف کنیم.»
سودو و تیمش به جای استفاده از نکروز برای از بین بردن سلولهای سرطانی، یک روش نوری برای تنظیم مرگ سلولی آپوپتوز ایجاد کردند - فرآیندی که طی آن سلولهای ناخواسته به طور فعال کشته میشوند تا ارگانیسم زنده بماند. محققان با کنترل pH درون سلولی با پروتئین های پمپ پروتون جاذب نور از خانواده رودوپسین به آپوپتوز رسیدند.
سودو گفت: «ما فکر میکردیم که اگر بتوانیم آپوپتوز را در سلولهای سرطانی هدف با استفاده از پروتئینها به جای مواد شیمیایی القا کنیم، میتوانیم به پیشرفتی در درمان سرطان بدون عوارض جانبی همراه کمک کنیم.»
به عنوان بخشی از یک رویکرد نوری برای درمان سرطان که توسط تیمی در دانشگاه اوکایاما توسعه یافته است، AR3، یک پروتئین فعال شده با نور از خانواده رودوپسین، در داخل سلول های سرطانی سنتز می شود و سپس نور اعمال می شود و آپوپتوز سلولی را القا می کند. با حسن نیت از دانشگاه اوکایاما و JST.
محققان بر روی آرکائرودوپسین-3 (AR3)، یک پروتئین جاذب نور از دسته رودوپسین تمرکز کردند که توانایی پمپ کردن یون های هیدروژن را به بیرون از سلول نشان داده است. با کاهش غلظت یون هیدروژن سلول، سلول قلیایی تر می شود. و قلیایی شدن سلول می تواند باعث آپوپتوز شود.
بر اساس این دانش، گروه تحقیقاتی شروع به آزمایش سلولها کردند تا ببینند آیا میتوان آنها را با استفاده از AR3 برای القای آپوپتوز به اندازه کافی قلیایی ساخت. محققان AR3 را در سلول های مشتق از سرطان انسان سنتز کردند و سپس سلول ها را در معرض نور سبز با طول موج تقریبی 550 نانومتر قرار دادند.
انقباض ناشی از قلیایی شدن سلول های HeLa انسانی که در pH 9.0 کشت شده بودند به طور قابل توجهی توسط AR3 فعال شده با نور تسریع شد. محققان مشاهده کردند که بیشتر سلول ها در عرض سه ساعت تحت آپوپتوز قرار گرفتند.
محقق Shin Nakao، یکی از دانشجویان سودو، آزمایشی موازی انجام داد که در آن شرایط pH اعمال شده روی سلول ها در pH فیزیولوژیکی خنثی 7.4 بود. یک تجزیه و تحلیل بیوشیمیایی نشان داد که قلیایی شدن داخل سلولی ناشی از AR3 مسیر سیگنالینگ آپوپتوز میتوکندری را تحریک می کند که منجر به مرگ سلولی همراه با تغییرات مورفولوژیکی می شود.
PH اندازه گیری غلظت یون هیدروژن در یک محیط است و به عنوان شاخص اسیدیته، خنثی بودن و قلیاییت استفاده می شود. سودو گفت: "من فکر می کردم که آزمایش رویکرد ما قطعا نمی تواند در شرایط خنثی انجام شود." سلولها وقتی در محلول قلیایی خیسانده میشوند میمیرند و من فکر کردم که آیا میتوان این فرآیند را با استفاده از AR3 تسریع کرد. بنابراین، من فقط در pH 9 (قلیایی) آزمایش کردم. با این حال، دانشآموز آزمایشی را با pH 7 (خنثی)، یعنی شرایطی که معمولاً در بدن انسان رخ میدهد، انجام داد.
در PH خنثی، مشاهده نتایج در مدت زمان طولانیتری ضروری بود، اما آزمایش در نهایت موفق شد. سودو گفت: "اگر استراتژی ما در pH خنثی عمل کند، می توان از آن برای توسعه درمان استفاده کرد."
ناکائو افزود: «من میخواستم شرایط را برای بیماران قابل اجرا کنم، کاری که در pH 9 قابل انجام نیست. "بنابراین، من رویکردمان را در pH 7 امتحان کردم. این اتفاق افتاد، بنابراین خوشحالم که آن را امتحان کردم."
سپس محققان رویکرد خود را در آزمایشهای in vivo آزمایش کردند. آنها AR3 را روی نورون های حسی C. elegans سنتز کردند و فقط سلول های عصبی را هدف قرار دادند. هنگامی که بدن C. elegans در معرض نور سبز قرار گرفت، تنها نورونهایی که AR3 را سنتز میکنند، واکنش حسی کاهشیافتهای به مواد شیمیایی نشان دادند. به نظر میرسد که یونهای هیدروژن توسط AR3 از این نورونها پمپ شده و باعث قلیایی شدن سلولها و مرگ آنها شده است.
بر اساس این نتایج، محققان به این نتیجه رسیدند که AR3 میتواند باعث آپوپتوز در سلولهای هدف در هنگام قرار گرفتن در معرض نور شود.
محققان رویکرد خود را در قلیاییسازی سلولها با روشی که واکسن پیامرسان RNA (mRNA) برای COVID-19 کار میکند، مقایسه میکنند. همانطور که mRNA برای سنتز پروتئین های لازم به سلول ها تزریق می شود، ژن های AR3 باید به سلول های سرطانی وارد شوند تا سلول ها بتوانند AR3 را سنتز کنند. نشانگرهای ژنتیکی را می توان تنها برای سنتز AR3 در سلول های هدف استفاده کرد.
سودو گفت: "با استفاده از روش آپوپتوز سلولی القا شده توسط نور، که در آن AR3 فقط در سلول های سرطانی انسان سنتز می شود، می توان سلول های بیمار را بدون ایجاد واکنش های نامطلوب در سلول های سالم اطراف از بین برد."
این گروه گفت که قصد دارد روی بافت پستانداران آزمایش کند. رویکرد محققین به آپوپتوز ناشی از عکس پتانسیل بهعنوان یک ابزار اپتوژنتیک برای از بین بردن انتخابی سلولهای هدف با وضوح فضایی و زمانی بالا دارد.
برخی از مردم ممکن است فکر کنند که چون رویکرد ما سرطان را با نور از بین میبرد، مانند روشهای قبلی است. با این حال، استراتژی ما حول آپوپتوز به جای نکروز متمرکز است و بنابراین اساساً متفاوت است. سودو گفت: رویکرد ما میتواند به روشهای درمانی کاملاً جدید منجر شود.